
問1
過程 A → B においては定積変化であるので、気体の状態方程式を考えると
$$p V = n R T$$
より $V$ が一定であれば、圧力 $p$ と温度 $T$ は比例する。
すなわち、温度は上がる。気体の体積は変わっていないので、外部から熱を吸収したために起こる温度上昇である。
また、気体の内部エネルギーは温度に比例するので、気体の内部エネルギーは増加する。
従って、答えは①となる。
問2
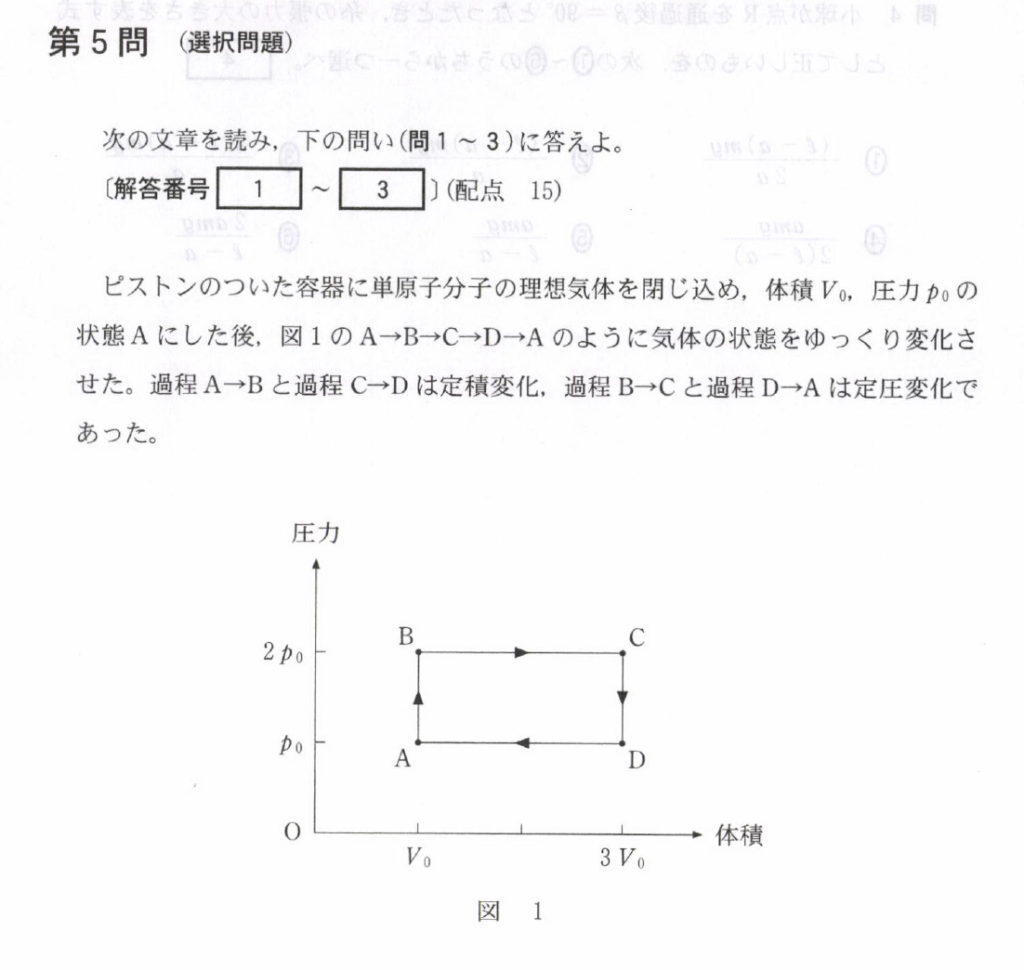
過程 A → B → C → D → A の間に気体が外部にした仕事の総和は四角形ABCDで囲まれる面積であるので $$2 p_0 V_0$$
となる。従って、答えは③となる。
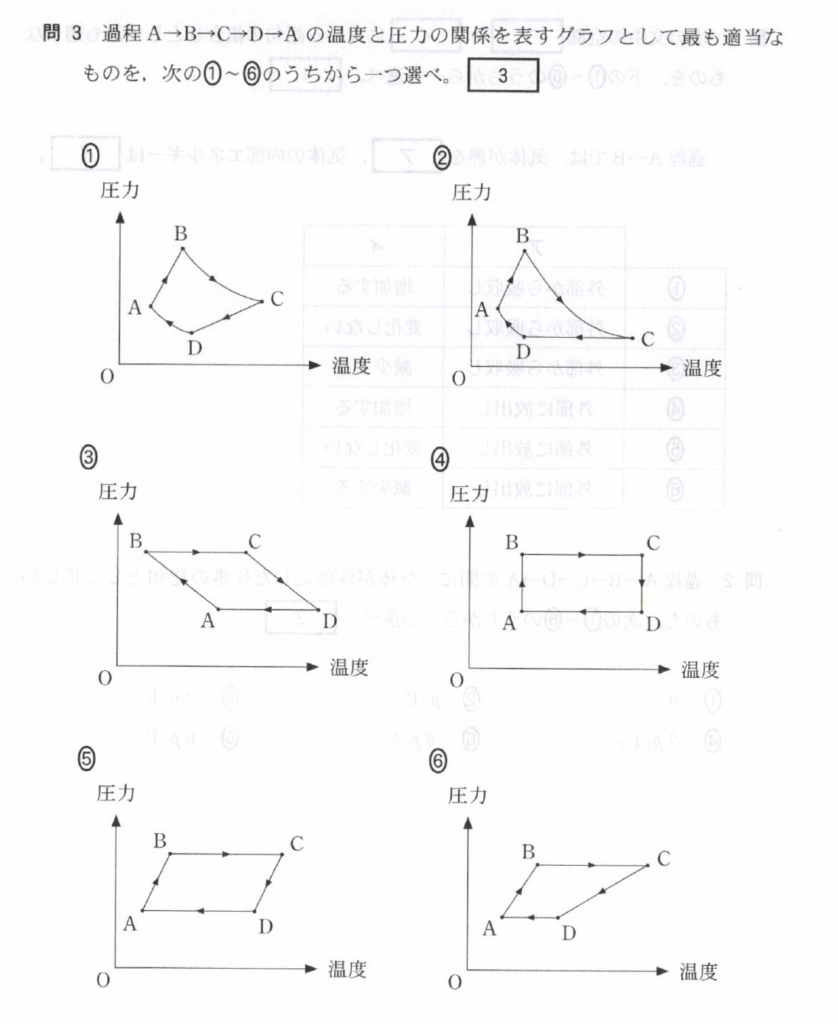
問3
まず、過程 A → B と過程 C → D を考えると、このとき等積変化であるので
\begin{align}
p V &= n RT \\
p &= \frac{n R}{V} T
\end{align}
より、原点を通る直線となる。
次に、過程 B → C と過程 D → A を考える。
この時は等圧変化であるので横軸と並行な直線となる。
これらから適切な $p-T$ グラフの形は⑥となる。